
様々な情報をお届けします
コラム
2022.11.29
『いわゆる「健康食品」と呼ばれるものについては、法律上の定義は無く、医薬品以外で経口的に摂取される、健康の維持・増進に特別に役立つことをうたって販売されたり、そのような効果を期待して摂られている食品全般を指しているものです。』1
このいわゆる「健康食品」には、一般食品の一部と保険機能食品が該当しており、この分類を議論するためには、どのような定義でヒトが摂取するものが分類されているのか理解する必要があります。ここでは、健康食品にフォーカスし、ヒトが摂取するものの区分の定義に加え、健康食品市場の変遷と機能性表示制度について、解説していきます。
口から摂取する物を大別すると食品と医薬品に分類されます。この分類の基準は、食品衛生法 (昭和二十二年法律 第二百三十三号)2 および食品安全基本法 (平成十五年法律第四十八号)3 に次のように定義されています。
第四条 この法律で食品とは、全ての飲食物をいう。ただし、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)に規定する医薬品、医薬部外品及び再生医療等製品は、これを含まない。
第二条この法律において「食品」とは、全ての飲食物(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)に規定する医薬品、医薬部外品及び再生医療等製品を除く。)をいう。
つまり、食品は医薬品や医薬部外品を除くすべての飲食物と定義されます。したがって、食品を分類するためには、医薬品や医薬部外品の定義を知る必要があります。医薬品、医薬部外品については、医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律 (昭和三十五年法律第百四十五号)4 (以下、「薬機法」とする) に以下のように規定されています。
第二条この法律で「医薬品」とは、次に掲げる物をいう。
- 一 日本薬局方に収められている物
- 二 人又は動物の疾病の診断、治療又は予防に使用されることが目的とされている物であって、機械器具等(機械器具、歯科材料、医療用品、衛生用品並びにプログラム(電子計算機に対する指令であって、一の結果を得ることができるように組み合わされたものをいう。以下同じ。)及びこれを記録した記録媒体をいう。以下同じ。)でないもの(医薬部外品及び再生医療等製品を除く。)
- 三 人又は動物の身体の構造又は機能に影響を及ぼすことが目的とされている物であって、機械器具等でないもの(医薬部外品、化粧品及び再生医療等製品を除く。)
- 2 この法律で「医薬部外品」とは、次に掲げる物であって人体に対する作用が緩和なものをいう。
- 一 次のイからハまでに掲げる目的のために使用される物(これらの使用目的のほかに、併せて前項第二号又は第三号に規定する目的のために使用される物を除く。)であつて機械器具等でないもの
- イ 吐きけその他の不快感又は口臭若しくは体臭の防止
- ロ あせも、ただれ等の防止
- ハ 脱毛の防止、育毛又は除毛
このように、薬機法に記載されている医薬品、医薬部外品の定義から外れた飲食物が食品と分類されます。
そして、食品は保健機能食品と一般食品に分類され、機能性表示ができるかどうかの有無で分類されます。この保健機能食品に特定保健用食品(トクホ) や栄養機能食品、機能性表示食品が含まれています。
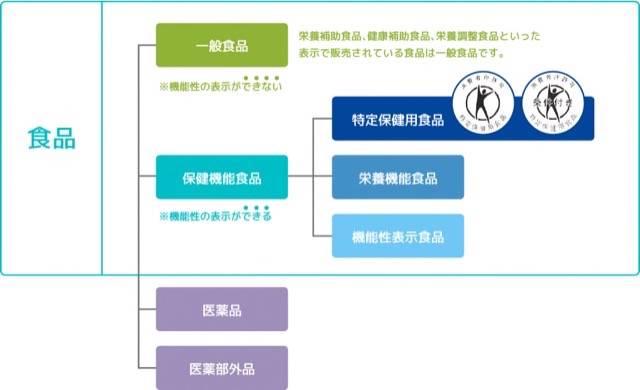
出典:「『機能性表示食品』って何?」 (消費者庁)5 を加工して作成
前述したように、特定保健用食品 (トクホ) や栄養機能食品、機能性表示食品が保健機能食品に分類され、「健康食品」に含まれます。このセクションでは、それぞれの保健機能食品の歴史と概要について紹介していきます。
1984年に文部省 (現:文部科学省) 特定研究「食品機能の系統的解析と展開」が実施されました。これにより、食品の三次機能 (体調調節) が提唱され、はじめて「機能性食品」という定義が示されました。その後、「食品の生体調整機能の解析」の研究推進 (1988年) や「機能性食品懇談会」の発足(1988年)、「機能性食品検討会」の発足 (1990年) を経て、1991年に特定保健用食品表示許可制度が施行され、「特定保健用食品」が生まれました。2001年には、「保険機能食品 (栄養機能食品、特定保健用食品)」制度が施行され、2015年の「食品表示法の施行に伴い機能性表示制度がはじまり、今の保健機能食品の体制に至ります。
特定保健用食品は、からだの生理学的機能などに影響を与える保健効能成分(関与成分)を含み、その摂取により、特定の保健の目的が期待できる旨の表示をする食品です。審査においては、食品ごとに消費者庁が審査をします。また、様々な条件が課せられており、「有効性の証明には、査読付きの研究雑誌への掲載」、「決められた試験機関での、関与成分の含有量の分析試験」などが必要となります。
| 項目 | 特定保健用食品 |
|---|---|
| 認証方式 | 個別許可型 |
| 機能性表示 できる成分 |
体の中で成分がどのように働いているか、という仕組みが明らかな成分 |
| 可能な 機能性表示 |
健康の維持、増進に役立つ、又は適する旨を表示 (疾病リスクの低減に資する旨を含む。) |
| 判別ポイント | トクホマークの表示 |
出典: 令和2年度健康食品取扱事業者講習会テキストより改変
人の生命・健康の維持に必要な特定の栄養素の補給のために利用されることを目的とした食品です。栄養素の名称と機能だけでなく、「日本人の食事摂取基準」に基づいた一日の摂取目安量(上限・下限量)や摂取上の注意事項も表示する義務があります。ただし、国が決めた基準に沿っていれば、許可や届出等の必要がなく、食品に含まれている栄養成分の栄養機能を表示することができます。
| 項目 | 栄養機能食品 |
|---|---|
| 認証方式 | 自己認証 |
| 機能性表示 できる成分 |
|
| 可能な 機能性表示 |
栄養成分の機能の表示(国が定める定型文) |
| 判別ポイント | 「栄養機能食品(◎◎)」の表示 ※◎◎は栄養成分の名称を記載 |
出典: 令和2年度健康食品取扱事業者講習会テキストより改変
特定保健用食品と同様に保健機能を表示することができる食品です。しかし特定保健用食品と異なり、消費者庁長官の個別の許可を受けたものではなく、事業者の責任で保健機能を表示します。その保健機能の有効性の科学的根拠や安全性などの情報を事業者が消費者庁へ「届出」を行うことが決められています。
| 項目 | 機能性表示食品 |
|---|---|
| 認証方式 | 事前届出制 |
| 機能性表示 できる成分 |
体の中で成分がどのように働いているか、という仕組みが明らかな成分 |
| 可能な 機能性表示 |
健康の維持、増進に役立つ、又は適する旨を表示 (疾病リスクの低減に資する旨を除く。) |
| 判別ポイント | 「機能性表示食品 届出番号△△」の表示 ※△△は消費者庁より与えられた番号を記載 |
出典: 令和2年度健康食品取扱事業者講習会テキストより改変
健康食品全体の市場規模は、年々微増を続けております。特定保健用食品および機能性表示食品の市場規模の変化に着目していくと、『特定保健用食品』の市場規模はわずかに右肩下がりとなり、機能性表示食品は年々拡大しております。
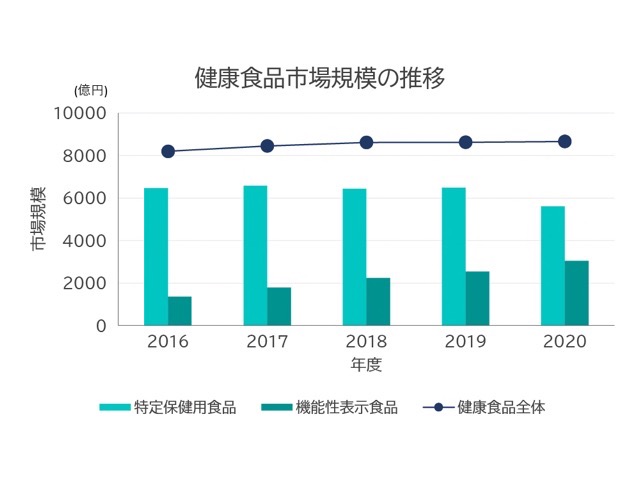
参考: 健康食品市場に関する調査を実施(2022年) | 株式会社矢野経済研究所9
参考: 特定保健用食品の市場および表示許可の状況 | 公益財団法人 日本健康・栄養食品協会10
また、特定保健用食品の許可数および機能性表示の届出数に着目すると、2017年に累計数が逆転し、機能性表示の届出数が特定保健用食品の許可数を上回りました。2020年においては、特定保健用食品の許可数が1071件、機能性表示の届出数が約4000件となり大きく差をつける状況となっています。
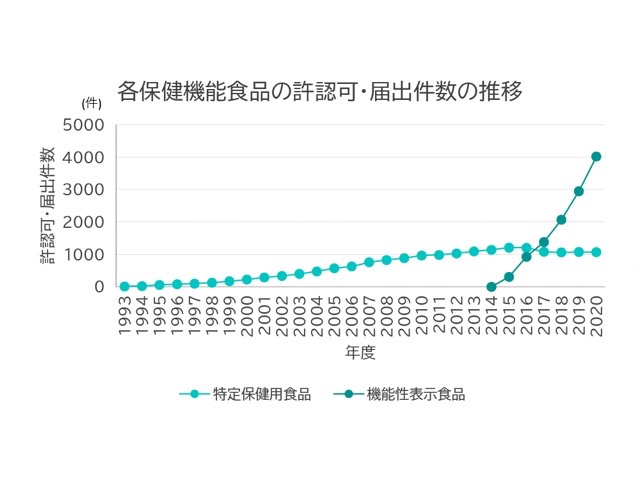
参考: 特定保健用食品の市場および表示許可の状況 | 公益財団法人 日本健康・栄養食品協会10
参考: 機能性表示食品の届出情報検索 | 消費者庁11
このように、機能性表示食品の市場が届出件数からも見て取れており、多くの企業が機能性表示食品の開発に力を入れていることが示唆されます。そこで、次のセクションでは、機能性表示食品について、解説していきます。
どの保険機能食品についても言えることですが、機能性について表示するためには、科学的根拠が必要となります。この科学的根拠の評価について、機能性表示食品の届出では、最終製品を用いたヒト臨床試験での評価に加え、最終製品または機能性関与成分のシステマティックレビューの評価が認められています。
前述したように、機能性表示食品の届出では、機能性の科学的根拠を評価するための方法が2種類あります。まず、最終製品を用いたヒト臨床試験での評価は、独自性の高い機能性を表示できる可能性があり、その機能性表示の先駆者として、市場を牽引する事ができると考えられます。一方で、最終製品または機能性関与成分のシステマティックレビューの評価の場合、ヒト臨床試験を実施する事と比較すると費用が抑えられ、商品の付加価値を向上する事が可能です。
オルトメディコは、機能性表示を目指したヒト臨床試験の設計・運営から、機能性表示の届出までサポートが可能です。ご興味がございましたら、お気軽にお問い合せ下さい!

ヒト臨床試験 (ヒト試験)
各種サポート業務等
各種お問い合わせは
お気軽にどうぞ
03-3812-0620 平日 | 9:00-17:00